


在第67届美国血液学会(ASH)年会上,陆道培医院陆佩华院长、张弦主任展示了一项基于“自然选择”平台的CD7 CAR-T疗法在复发/难治性CD7阳性血液系统恶性肿瘤中的大规模临床研究。该研究成果不仅验证了NS7CAR-T在T-ALL/LBL、AML、MPAL及PTCL中的广泛适用性,也为移植后复发患者提供了创新治疗选择,具有潜在变革性临床价值,为未来治疗策略优化与精准管理提供了重要循证依据。

标题:CD7 CAR-T cell therapy based on “Natural Selection” for the treatment of Relapsed or Refractory CD7-positive Hematologic Malignancies: A large cohort study
中文标题:基于“自然选择”平台的CD7 CAR-T细胞治疗复发/难治性CD7阳性血液系统恶性肿瘤:一项大样本队列研究
第一作者:张弦
通讯作者:陆佩华
研究背景
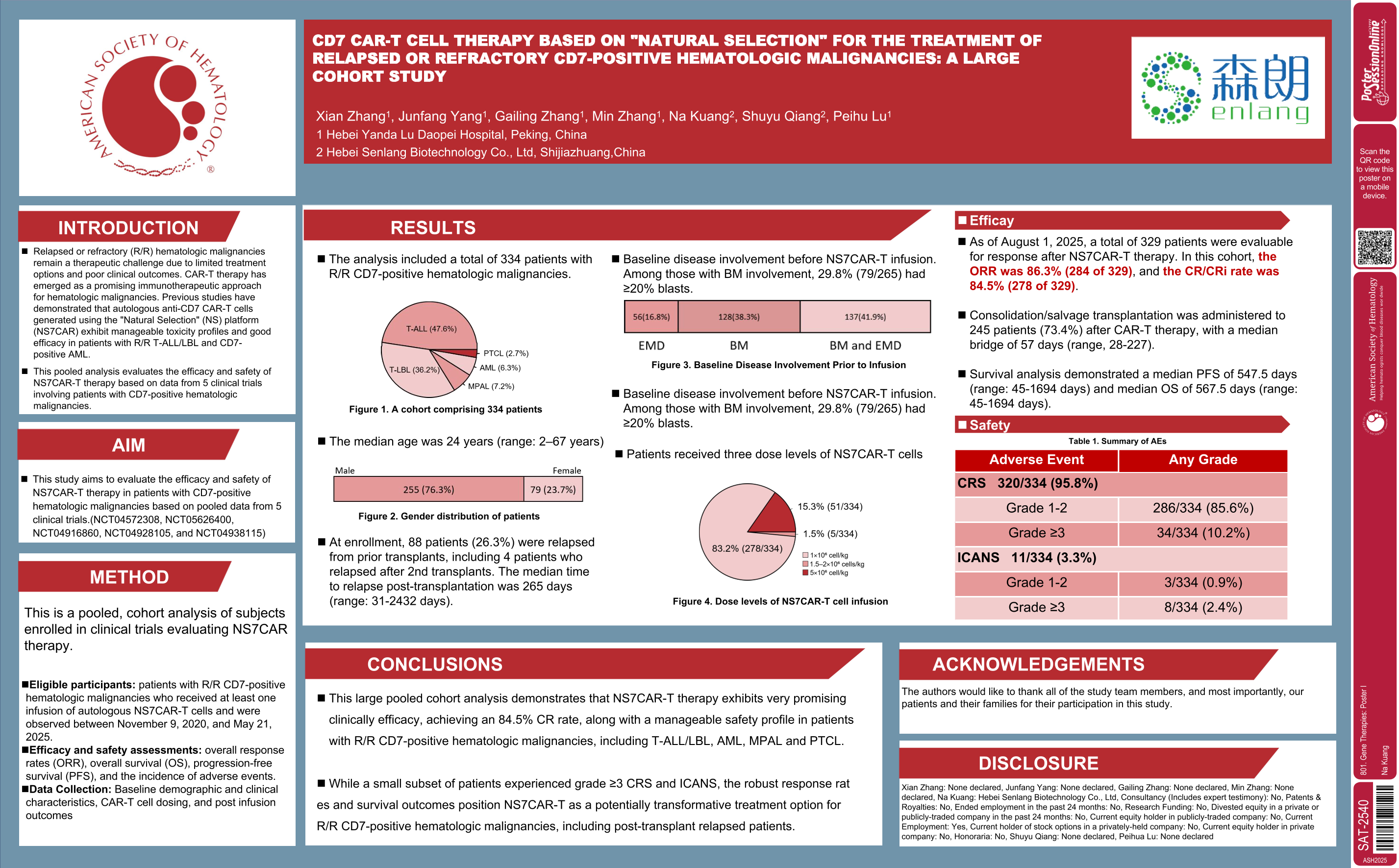
复发/难治性(R/R)血液系统恶性肿瘤,包括T细胞急性淋巴细胞白血病/淋巴母细胞淋巴瘤(T-ALL/LBL),由于治疗选择有限且临床预后较差,仍是治疗难题。嵌合抗原受体T细胞(CAR-T)疗法已成为一种有前景的免疫治疗手段。既往研究表明,基于“自然选择”(Natural Selection, NS)平台制备的自体抗CD7 CAR-T细胞(NS7CAR)在R/R T-ALL/LBL及CD7阳性急性髓系白血病(AML)患者中展现出可控的毒性反应和良好的疗效。本研究汇总分析了5项临床试验(注册号:NCT04572308、NCT05626400、NCT04916860、NCT04928105、NCT04938115)中接受NS7CAR-T治疗的CD7阳性血液肿瘤患者的疗效与安全性数据。
研究方法
本研究为一项汇总性队列分析,纳入了在上述临床试验中接受至少一次自体NS7CAR-T细胞输注的R/R CD7阳性血液系统恶性肿瘤患者,观察时间为2020年11月9日至2025年5月21日。系统收集了基线人口学与临床特征、CAR-T细胞剂量及输注后结局。疗效与安全性评估指标包括总体缓解率(ORR)、总生存期(OS)、无进展生存期(PFS)及不良事件发生率。
研究结果
共纳入334例R/R CD7阳性血液系统恶性肿瘤患者,其中T-ALL 159例(47.6%)、T-LBL 121例(36.2%)、混合表型急性白血病24例(7.2%)、AML 21例(6.3%)、外周T细胞淋巴瘤9例(2.7%)。中位年龄24岁(2–67岁),男性255例(76.3%),女性79例(23.7%)。88例(26.3%)患者为既往移植复发,包括4例二次移植复发。骨髓受累者中,29.8%(79/265)具有≥20%原始细胞。患者接受三种剂量的NS7CAR-T细胞输注,中位剂量为1×10⁶ cells/kg。
截至2025年8月1日,329例可评估患者中ORR为86.3%(284/329),完全缓解/完全缓解伴不完全血液学恢复(CR/CRi)率为84.5%(278/329)。245例(73.4%)患者在CAR-T治疗后接受巩固/挽救性移植,中位间隔57天(28–227天)。中位PFS为547.5天(45–1694天),中位OS为567.5天(45–1694天)。安全性评估显示,细胞因子释放综合征(CRS)发生率为95.8%(320/334),其中85.6%为1-2级,10.2%为≥3级;免疫效应细胞相关神经毒性综合征(ICANS)发生率为3.3%(11/334),其中0.9%为1-2级,2.4%为≥3级。
研究结论
这项大样本汇总队列分析表明,NS7CAR-T疗法在R/R CD7阳性血液系统恶性肿瘤(包括T-ALL/LBL、AML、MPAL及PTCL)患者中展现出极具前景的临床疗效,完全缓解率高达84.5%,且安全性可控。尽管部分患者出现≥3级CRS或ICANS,但其整体反应率与生存结局均十分突出,提示NS7CAR-T有望成为R/R CD7阳性血液肿瘤患者(包括移植后复发者)的一种变革性治疗选择。
