

骨髓增生异常综合征(MDS)是一组起源于造血干细胞的克隆性疾病,既常见于老年人,又具有高度异质性:有的进展缓慢,主要影响生活质量;有的则可能在较短时间内进展为急性髓系白血病(AML),危及生命。
本期,陆道培医院造血干细胞移植科赵艳丽主任以通俗易懂的语言,系统梳理MDS在诊断、分型、预后评估与治疗决策方面的最新进展,把患者和家属最关心、也最容易困惑的几个问题说清楚:MDS是不是白血病?为什么有的人多年稳定,有的人却发展很快?是不是一确诊就要马上化疗?造血干细胞移植是不是唯一出路?
01MDS的流行病学特征
MDS中国发病率为(0.23~1.51)/10万,MDS发病率随年龄增长而增加,80%发病年龄大于60岁。因此,MDS本质上是一种以老龄患者为主要群体的疾病,这一特征对诊断策略、治疗选择及预后评估均具有重要影响。
02MDS的诊断
目前MDS的诊断主要参考国际通用的MDS-Vienna诊断体系:

我国对血细胞减少的诊断标准相对更严格:中性粒细胞绝对值<1.8×10⁹/L;血红蛋白<100g/L;血小板<100×10⁹/L。而WHO及ICC标准中,贫血和血小板减少的阈值更高。因此,中国MDS的诊断比例相对偏低,与更严格的血象标准密切相关。此外,ICC2022版指南强调:贫血是MDS诊断的重要必要条件之一,若不存在贫血,应重新审视MDS诊断的合理性。
此外,MDS诊断的确立需排除可能发展为MDS的前驱疾病,包括CHIP(潜质未定的克隆性造血)、ICUS(意义未明的特发性血细胞减少症)、CCUS(意义未明的克隆性血细胞减少症)、CMUS(意义未明的克隆性单核细胞增多症)。ICUS的诊断标准需要持续(≥4个月)一系或多系血细胞减少,与MDS区分的关键是:是否存在≥10%的病态造血、原始细胞增多,或MDS定义性染色体/分子异常。
03MDS的分型
1. FAB分型
1982年FAB分型主要基于形态学,曾将原始细胞上限定为30%。随着认识的进步,RAEB-t 等类型已被重新归类为急性髓系白血病,CMML 等疾病也被划入 MDS/MPN 类别。
2. WHO 2022分型
WHO分型将原始细胞界限下调至20%,并首次将部分特定遗传学异常作为独立亚型,包括:MDS伴5q缺失;MDS伴 SF3B1 突变;MDS伴双等位 TP53 突变。同时,WHO引入MDS-LB(低原始细胞)、MDS-IB(原始细胞增加)、MDS-h(低增生)MDS-f(纤维化)等新类别,并删除MDS-U,MDS-EB。
3. ICC 2022分型
ICC分型的重要创新是提出 MDS/AML(原始细胞10%–19%) 这一过渡类别,使部分生物学行为更接近AML的患者,更容易纳入AML相关临床试验;更早获得新药治疗及医保可及性。同时,ICC将既往“治疗相关性”或“继发性”疾病作为限定词而非独立分型,更强调遗传学对预后的决定性作用。
04MDS的预后评估
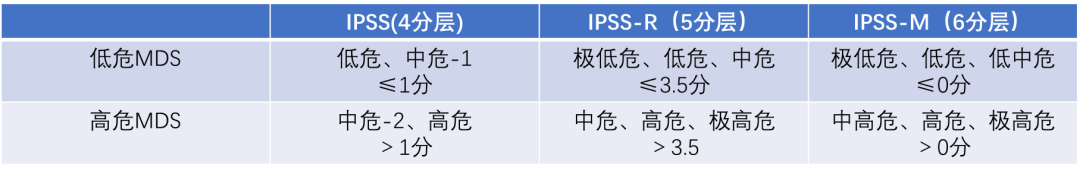
临床实践中,通常将患者简化分为低危MDS与高危MDS两大类,以指导治疗策略。IPSS-M(分子评分体系)于2022年提出,纳入31种常见基因突变,显著提高了危险分层的准确性。预后分层提示:无基因突变者预后最佳;SF3B1 次之;TP53 预后最差;值得注意的是,NPM1突变在MDS中预后不良(仅次于TP53),但在AML中属预后良好,临床需结合病史综合判断。
05MDS的治疗
自2004年阿扎胞苷获批以来,已有多种药物上市,包括:来那度胺、地西他滨、罗特西普、口服地西他滨、艾伏尼布以及一种端粒酶抑制剂(用于减少贫血)等。
1.低危MDS:
治疗目标:改善生活质量,减少输血依赖。
部分仅有血细胞减少但无明显症状患者可随访观察。
对有临床症状的血细胞减少(贫血、血小板减少、中性粒细胞减少),治疗以支持治疗为主,包括输血支持以及处理血细胞减少、感染和出血风险。
若上述治疗无效,可考虑低剂量去甲基化药物、造血干细胞移植或临床试验。
2.高危MDS:
治疗目标:追求长期无病生存,延缓向急性髓系白血病转化。
首先评估是否具备移植条件:所有高危MDS患者确诊后均应评估。
不适合移植者:考虑去甲基化药物维持治疗、临床试验或针对特定突变(如IDH1/2, FLT3)的靶向药物及新药临床试验等。
06造血干细胞移植(HSCT)在MDS中的应用
01哪些MDS患者需要考虑移植?
首先是否需要移植,取决于疾病本身的危险程度。对于中高危、高危或极高危的MDS患者来说,一旦明确诊断,就应尽早评估移植条件,而不是等药物治疗失败后再考虑。研究已经反复证实,这类患者越早移植,长期生存机会越大。
而对于一些被评估为“低危”的患者,如果出现,比如血细胞下降严重、需要反复输血;药物治疗效果不好甚至耐药;合并骨髓纤维化;发现与MDS相关的遗传易感基因或属于治疗相关MDS等,也需要重新考虑移植的必要性。
当然,是否能做移植也要综合患者自身情况,包括年龄、体力状态、心肺等重要脏器功能,以及是否合并其他严重疾病。现在临床上,一般认为80岁以下、身体状态尚可、重要脏器功能允许、合并疾病较少的患者,都可以接受移植评估。
02现在MDS移植多吗?安全吗?
过去十年,MDS移植数量显著增加,而且接受移植的患者平均年龄也在不断上升。这说明,越来越多的中老年患者,也从移植中获益。
在供者方面,同胞相合供者和非血缘相合供者最优,半相合(供者为父母、子女等)已经成为非常成熟、常规的方案,一般建议优选年轻供者(即使HLA匹配度稍差)。目前大多数中心还采用了以PTCY为核心的预防方案,使移植相关并发症明显减少,整体安全性大幅提高。
03移植什么时候做最好?
医生会结合包含基因信息在内综合评估移植时机,总体原则是风险越高,越要尽早移植。
对于风险较低的患者,可以在医生指导下观察,但对于60岁以上的低危患者,随着年龄增长和并发症增加,移植机会可能逐渐关闭,反而要适当放宽移植指征,提前规划。
04是不是一定要先把骨髓里的异常细胞降下来,才能做移植?
如果骨髓中原始细胞比例较高,移植前进行适当治疗,在一定程度上有助于降低复发风险。但对于原始细胞并不高的高危MDS患者,为了追求“残留为0”而长期用药、反复等待,反而可能延误最佳移植时机。
05年龄大了还能不能移植?
年龄确实会影响移植风险,但年龄并不是唯一标准。数据显示,年轻患者移植后的长期生存率更高,但近年来,65~79岁患者的移植效果也在持续改善。只要身体条件允许,很多老年患者同样可以安全完成移植,并获得长期获益。
06特殊情况:遗传因素和TP53突变
少部分MDS患者与遗传易感基因有关。这类患者往往对常规药物治疗反应较差,更需要尽早考虑移植。同时,在选择供者时,也需要筛查是否携带相同的遗传问题。
另外,带有TP53突变的MDS属于预后最差的一类。虽然联合药物治疗可以在短期内改善病情,但目前仍无法替代移植的作用。对这类患者来说,移植仍是唯一可能带来长期生存机会的治疗方式。
07移植后就“万事大吉”了吗?
移植后,需要继续通过微小残留病(MRD)监测,密切观察疾病是否有复发迹象。一旦发现异常,可以及时采取干预措施,如药物治疗、供者淋巴细胞输注,必要时甚至考虑二次移植。
目前还没有证据表明,所有患者在没有异常的情况下,提前使用药物进行“预防性治疗”可以提高生存率,因此是否用药需要个体化判断。对于微小残留阳性或复发的患者,移植后的治疗策略包括使用HMA和供体淋巴细胞输注(DLI)。
