

在急性B淋巴细胞白血病(简称急淋B)的治疗中,贝林妥欧单抗和CAR-T细胞治疗都是近年来广泛应用的细胞免疫治疗手段,尤其在患儿出现难治或复发时,常被作为第二线或挽救性治疗方案。然而,很多家长对这两种治疗方式的区别仍感到困惑:它们的作用机制有何不同?适用人群是否一样?在临床选择上应该如何权衡?
上海新道培医院副院长刘芳教授线上科普答疑,从治疗原理、优缺点、适用时机、疗效持续性以及治疗成本等几个方面,深入解析贝林妥欧单抗和CAR-T的异同,帮助家长们了解应该如何选择。
一、作用机制对比
01共同点
两者都靶向CD19抗原,旨在激活T细胞杀灭CD19阳性的恶性B细胞(包括白血病细胞)。
使用前都需通过流式细胞术或免疫组化检查,确认肿瘤细胞表达CD19。
02贝林妥欧单抗(Blinatumomab)
又称“双特异性T细胞接合抗体”(BiTE)。
分子结构上,一端结合肿瘤细胞的CD19,另一端结合T细胞的CD3。
当它把靶向CD19的肿瘤细胞与T细胞“牵”到一起时,会在人体内直接激活并扩增内源性T细胞,使其对CD19阳性的白血病细胞产生杀伤作用。
属于“成药”——药物制备好后即可使用,无需个性化生产或等待细胞培养。
03CAR-T细胞治疗
CAR-T是“嵌合抗原受体T细胞”(Chimeric Antigen Receptor T-cell)。
先从患者体内采集T细胞,然后通过基因工程手段将靶向CD19的CAR基因转入这些T细胞,使其表达具有识别CD19功能的受体。
将改造后的CAR-T细胞在体外扩增后回输给患者,遇到CD19阳性白血病细胞时,即可被强烈激活并快速扩增,发挥杀伤作用。
属于“现生产”(即个性化细胞制品),需要专门实验室进行培养和检测,整个过程通常需数周时间。
二、优缺点对比
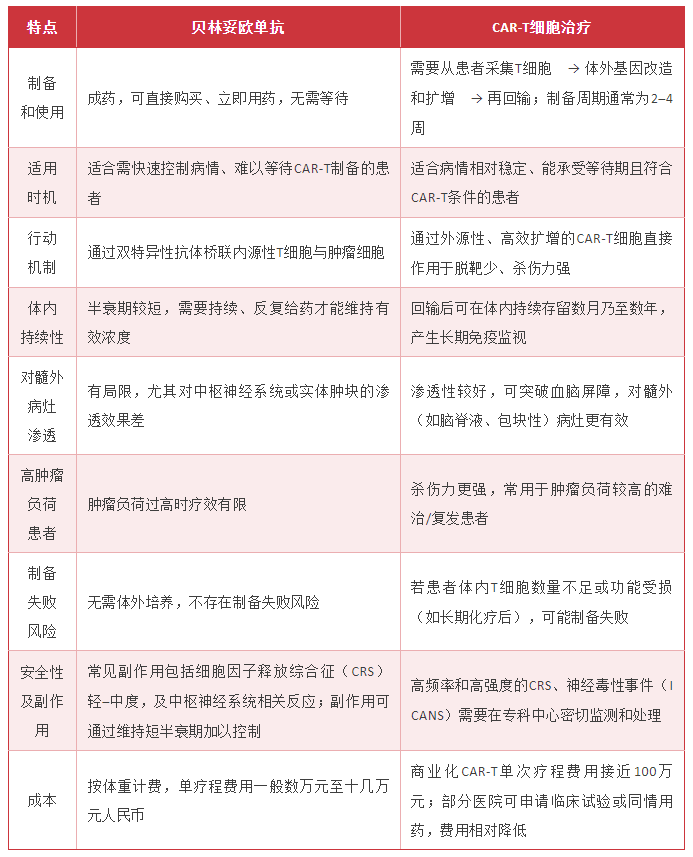
三、适应症及临床选择建议
下面根据不同临床场景,给出常见的选择指导意见。最终决策应在医生评估、家长知情同意和经济可承受能力等多方面综合考虑后做出。
01病情需要迅速控制、无法等待CAR-T制备的患者
如果白血病复发/难治后病情进展较快,无足够时间等待CAR-T的2–4周制备周期,先采用贝林妥欧单抗可以快速发挥免疫杀伤作用、控制病情。
适用于高危复发,且髓内、髓外负荷尚未十分巨大,但已有进展趋势的患者。
适用于临床需要尽快降瘤,以便后续其他治疗(如移植)。
02高肿瘤负荷或出现髓外病灶的患者
若患者体内肿瘤负荷极高(骨髓里 blasts 占比较高),或者已经出现中枢神经系统(CNS)或其他实体包块病灶,贝林妥欧单抗在高负荷或实体瘤渗透方面效果有限。
CAR-T在这一类患者中常表现出更强的降瘤能力和良好的髓外渗透性,更容易清除中枢神经病灶或包块。
适用于高肿瘤负荷、CNS浸润或其他髓外病灶(如皮下包块)。
适用于既往治疗方案效果差、需一次性打击大量残余病灶。
03患者免疫系统/淋巴细胞功能受损,难以制备CAR-T的情况
CAR-T需要从患者体内获得足够数量、功能正常的T细胞。
如果长期接受高强度化疗后,外周血淋巴细胞明显耗损,分离回收不到足够数量或功能低下的T细胞,就可能导致CAR-T制备失败。
这时,直接给予贝林妥欧单抗,不依赖体外改造,更适合免疫细胞严重受损的患者。
04将来有移植或其他治疗计划、需达到既定桥接目标的患者
如果患者计划后续进行造血干细胞移植,需要先将白血病病灶压低到MRD(最小残留病)或完全缓解状态。
贝林妥欧单抗可作为桥接治疗或巩固疗法,帮助降低病灶、获取移植机会。
若患者家庭具备足够经济条件,且在术前评估中免疫功能良好、等候时间可接受,CAR-T也可作为桥接到移植的强力降瘤手段,甚至在某些情况下替代移植取得长期生存。
05治疗目的与预期不同
贝林妥欧单抗更偏向“短期调控+维持”,通过持续给药保持低水平残余病灶控制,不太可能一针见效长期治愈。主要定位在:难治/复发时的降瘤+桥接移植;掌握病情波动、需要反复给药来维持疗效的患者。
CAR-T细胞治疗更偏向“一次性冲击+持久监测”,在多数适合症例中回输后可在体内存留数月甚至数年,具备较高的长期无病生存(EFS)和可达到治愈可能性。
四、常见副作用及管理
01贝林妥欧单抗
细胞因子释放综合征(CRS):多为轻度至中度,可出现发热、乏力、心动过速等。通过暂停输注、支持治疗或皮质类固醇可迅速缓解。
神经毒性(神经精神症状):包括头痛、困惑、抽搐等。大多可逆,需要严密监测,出现症状时可调整剂量或中断治疗。
因半衰期短,一旦停药不良反应可较快消退。
02CAR-T细胞治疗
CRS:发生率较高,轻度病例表现与贝利妥欧相似;重度病例可出现低血压、呼吸困难、脏器功能障碍等,需要IL-6拮抗剂(如托珠单抗)及重症监护。
神经毒性(ICANS):表现为意识障碍、癫痫样发作、脑水肿等,部分患者需抗惊厥药物、皮质类固醇及监护管理。
长期免疫缺陷:因CD19阳性B细胞被清除,部分患者可能出现感染风险增高,需要定期监测免疫球蛋白水平,必要时给予静脉免疫球蛋白替代治疗。
五、治疗费用及经济考量
01贝林妥欧单抗
按体重计费,在国内一疗程(28天)费用区间通常在几万元到十几万元人民币之间。
若疗程结束后需继续维持,可按周期续费,但总体费用相对CAR-T要低。
02CAR-T细胞治疗
商业化CD19 CAR-T(如河源生物“唯11”)在国内一次性费用接近100万元人民币。
部分医疗机构开展临床试验或同情用药项目,费用可大幅降低,但需满足相应条件并等待名额。
对于家庭经济承受能力有限的患者,需要与医生沟通,争取医保报销或临床试验机会。
总结与决策要点
1. 确认CD19表达
两种疗法都要先做流式细胞或免疫组化,确认白血病细胞表面有CD19阳性,才能考虑使用。
2. 评估患者病情进展速度、肿瘤负荷及髓外病灶
病情发展过快、肿瘤负荷尚可、需要短期控制,可首选贝利妥欧单抗。
高负荷、CNS或实体包块病灶,CAR-T更有优势。
3. 评估患者的免疫细胞状态
若患者长期化疗后淋巴细胞减少严重,CAR-T制备存在较大失败风险,可考虑贝林妥欧单抗。
免疫功能相对较好、可耐受等待期,则可优先考虑CAR-T。
4. 考虑等待期期间的病情风险
CAR-T制备周期一般需2–4周,若患者在此期间病情可能快速恶化,需要有过桥治疗(如贝林妥欧单抗)以控制病情、争取等待时间。
5. 评估家庭经济条件和支付途径
如果预算有限,可先使用贝林妥欧单抗;若有经济或慈善/医保支持,并且符合CAR-T适应证,就可直接选择CAR-T以期获得更持久的疗效。
6. 后续治疗计划
若计划后续进行造血干细胞移植,可根据桥接需求选择:短期桥接可选贝林妥欧,若想缩小病灶、争取不移植也能长期缓解,可考虑CAR-T。
对于部分无法进行移植的儿童,如果条件允许、家庭意愿强烈,也可以CAR-T作为“最后一搏”,因为CAR-T的长期无病生存机会较高。
两种细胞免疫治疗各有优劣,没有绝对的“最佳”方案,关键在于结合每个患儿的具体病情、免疫状态、等待时间、经济条件以及后续治疗计划,综合评估后与主治医生充分讨论,做出最适合的决策。
专家介绍

刘芳 教授
主任医师、上海新道培血液病医院医疗副院长
四川省女医师协会血液专业委员会常务委员
四川省妇幼保健协会第一届脐带血应用专业委员会常务委员非公立医疗机构协会血液病专委会委员中国妇幼保健协会脐带血应用委员会委员2016年在美国iCellgene 学习CAR-T细胞培养技术。
从事造血干细胞移植近20年,作为独立医疗组长累积完成造血干细胞移植超过700例,其中大部分为单倍体相合移植,对预防复发和处理并发症积累了丰富的经验。
主持多项CAR-T细胞治疗临床试验,世界首次完成CLL1-CD33复合CAR-T治疗难治复发AML,世界首次完成BCMA-CD19复合CAR-T治疗自身免疫相关的疾病,成果在2018年EHA、2018ASH、2019年iw-CAR、2019年ASH,2020 EHA 、2022年iwAL大会发言、被评为2018 EHA最佳摘要、2020年EHA白血病版块best of EHA。
